Понятие о водородном показателе рн школьный уровень. Водородный показатель кислотности (рН). pH в крови артериальной и венозной, плазме и сыворотке
Уровень активности ионов водорода в воде является одним из важнейших факторов, влияющих на оценку качества жидкости. Именно от данного критерия зависит уровень кислотно-щелочного баланса и направленность биохимических реакций, которые будут происходить в организме после употребления этой жидкости. В данной статье мы подробнее остановимся на вопросе, что такое pН воды, каким образом его определяют, а также же как повысить или понизить pН воды.
Из этой статьи вы узнаете:
Что такое pН воды
Какова норма pН воды
Чем грозит низкий уровень pH воды
Как измерить pН воды
Что такое pН воды
Показатель pH является единицей активности иона водорода, которая равна обратному логарифму активности водородных ионов. Так, например, вода, pH которой составляет 7, обладает 10–7 моль на один литр ионов водорода. Следовательно, жидкость с pH равном 6 – 10–6 моль на один литр. Шкала показателей pH при этом варьирует в диапазоне от 0 до 14. Если pH воды менее 7, то она является кислой, а если более 7 – тогда щелочной. Норма pH для поверхностных водных систем составляет 6,5–8,5, для подземных – 6–8,5.
Показатель pH воды равняется 7 при 25 °С, но при взаимодействии с диоксидом углерода в атмосфере данное значение будет составлять 5,2. Уровень pH тесно связан с атмосферным газом и температурой, поэтому воду следует проверить в самые короткие сроки. pH воды не сможет дать полной характеристики и повода для ограничения подачи воды.
Когда в воде растворяются различные химические вещества, то данный баланс подлежит изменению, что, в свою очередь, провоцирует изменение показателя pH. Если в воду добавить кислоту, концентрация ионов водорода возрастает, и концентрация гидроксид-ионов, в свою очередь, понижается. Если в жидкость добавить щелочь, тогда концентрация гидроксид-ионов возрастает, а содержание ионов водорода понижается.
Уровень pН воды показывает уровень кислотности или щелочности среды, а кислотность и щелочность характеризуется количественным содержанием в воде элементов, нейтрализующих щелочь и кислоту. Так, например, температура отражает уровень нагрева вещества, но не количественный показатель тепла. Если мы коснемся воды рукой, то мы определим, теплая она или холодная, но мы не сможем сказать, какое количество тепла в ней содержится (другими словами, сколько потребуется времени для того, чтобы вода остыла).
Показатель pH – один из основных качественных характеристик воды. Он отражает кислотно-щелочной баланс и определяет, каким образом будут происходить те или иные биологические и химические процессы. Величиной pH воды определяется скорость протекания той или иной химической реакции, уровень коррозионной агрессивности жидкости, степень токсичности загрязняющего вещества и многие другие факторы. Более того, кислотно-щелочной баланс среды организма определяет наше состояние здоровья, настроение и самочувствие.
Различают следующие группы воды, в зависимости от показателя pH:
Контролировать уровень pН воды необходимо на каждом этапе очистки жидкости, поскольку смещение баланса может негативно отразиться на вкусовых качествах, запахе и оттенке воды, а также снизить эффективность ее очистки.
Каков нормальный pН воды
Из-за стремительного темпа современной жизни, неправильного питания, нарушения пищевого и питьевого режимов уровень pН в организме человека падает. Так, кислотно-щелочной баланс смещается в сторону повышенной кислотности (pН до значения 7 подразумевает кислую среду, и до 14 – щелочную, соответственно, чем ниже данный уровень, тем выше кислотность), что может привести к серьезным заболеваниям. Решать эту проблему можно с помощью ежедневного употребления минеральной воды с оптимальным уровнем активности ионов водорода. Именно поэтому важно знать, какая величина pН является нормой для воды, которую вы регулярно употребляете в пищу.

Итак, какой должен быть pН воды? Профессионалы утверждают, что эта величина должна ориентировочно соответствовать нормальному показателю pН крови человека (7,5). Именно поэтому для питьевой воды норму pН рассчитывают от 7 до 7,5. Благодаря чистой питьевой воде с нормальным показателем активности ионов водорода улучшаются обменные процессы в организме, увеличивается общая продолжительность жизни и оптимизируется обмен кислорода. И наоборот, из-за сладких, газированных и содержащих красители напитков уменьшается pН человеческой крови, что можно сразу заметить по неприятной сухости во рту.
Поэтому лучше всего отдавать предпочтение воде с «правильным» показателем pН. Вы всегда сможете найти эту информацию на этикетке любой бутылки. Никакой фильтр с наполнителями и абсорбентами не сможет заменить настоящую природную воду с оптимальным уровнем pН. Некоторые пытаются понизить кислотность воды pН и придать жидкости полезные свойства, добавляя лимонный или огуречный сок, тем не менее это далеко не всегда оказывает должный эффект. Еще один известный способ изменения pН воды – это электролиз, который позволяет получить в двух емкостях щелочную и кислую воду. Щелочная вода с высоким pН считается «живой», ее используют для лечения, а кислая – «мертвой», которую чаще всего используют для умывания.
Тем не менее такие способы не подойдут для ежедневного использования. В этой ситуации остается только одно рациональное решение – отдать предпочтение слабоминеральной природной воде с необходимым для здоровья уровнем кислотности.
Измерение pН воды
Не стоит забывать о том, что человеческий организм на целых 70 % состоит из воды! Продукты обмена веществ в клетках представляют собой кислоты, в то время как основная масса внутренних жидкостей организма, за исключением желудочной кислоты, слабощелочные. Особое значение при этом имеют показатели крови. Организм человека нормально функционирует, если его кровь слабощелочная, и величина ее pН составляет от 7,35 до 7,45.
В том случае, когда в кровь и межклеточную жидкость попадает большое количество кислот, происходит нарушение кислотно-щелочного баланса. Даже небольшое отклонение уровня pН от данных показателей (от 7,35 до 7,45) может привести к серьезному нарушению здоровья. Если продолжается процесс повышения кислотности крови и дальнейшее понижение значения pН до 6,95, то наступает кома и возникает настоящий риск для жизни человека! Именно по этой причине необходимо отслеживать величину pН питьевой воды, которая является одной из важнейших показателей ее качества!
- Лакмусовая бумага.
Уровень pН воды вы сможете определить самостоятельно, в домашних условиях. В качестве прибора для измерения pН воды вы можете использовать лакмусовую (индикаторную) бумагу, которая меняет свой оттенок при кратковременном погружении в изучаемую среду. Так, при погружении в кислотную среду лакмусовая полоска приобретает красный оттенок, а в щелочную – синий. Далее следует сравнить получившийся цвет с цветной шкалой, в которой для каждого оттенка соответствует конкретный уровень pН, чтобы определить данный показатель у исследуемой жидкости. Данный метод определения pН является самым простым и дешевым.
- РН-метр.
Для наиболее точного определения уровня pН используют pН-метр для воды. Данный прибор для определения pН воды более дорогостоящий, чем лакмусовая бумага, тем не менее он определяет уровень pН жидкости в точности до сотых!
РН-метры для воды бывают бытовыми (портативными) и лабораторными. Чаще всего используют первый вариант, мы остановимся на них подробнее. Они различаются:
Степенью защиты от воды.
Наличием (или отсутствием) автоматической калибровки.
Точностью результатов.
Последний параметр определяется количеством калибруемых точек (1 или 2). Точками называют буферные растворы, с помощью которых и производят калибровку РН-метра. Рекомендуем приобрести прибор с автоматической калибровкой.
- Самодельные тест-полоски.
Существуют специальные тест-полоски, определяющие уровень pН-среды. Такие полоски очень удобны в использовании. Их упаковка оснащена шкалой, с помощью которой определяют концентрацию водородных ионов. Но такие тест-полоски не так часто появляются в продаже, при этом они довольно дорогостоящие.
При всех своих преимуществах pН-метры для воды также отличаются сравнительно высокой ценой.
Вы можете воспользоваться самодельными тест-полосками, чтобы определить pН воды.
Существуют различные вещества, которые меняют свой цвет в зависимости от содержания водородных ионов в жидкости. Например, чай вместо коричневого оттенка приобретает желтый, если в него добавить ломтик лимона.
Таким же образом меняют свой цвет, в зависимости от содержания водородных ионов, вишневый, смородинный соки и т. д. В природе существует огромное количество таких органических индикаторов. И на основе таких индикаторов создают самодельные тест-полоски, которые позволяют определить pН воды.
Мы воспользуемся веществом, входящим в состав красной цветной капусты. Данный овощ содержит пигмент anthocyanin, относящийся к категории флавоноидов. Именно он отвечает за оттенок сока капусты и меняет его, в зависимости от уровня кислотности.
Антоцианы в кислой среде приобретают красный оттенок, а в щелочной – синий, в фиолетовый они окрашиваются, находясь в нейтральной среде. Аналогичными свойствами обладает и пигмент свеклы.
Для проведения эксперимента вам потребуется половина качана красной цветной капусты среднего размера, который следует мелко нарезать. Затем нарезанную капусту необходимо положить в емкость и залить литром воды. Затем вскипятите воду и оставьте данное зелье вариться в течение 20–30 минут.
За это время часть жидкости испарится, и вы получите отвар насыщенного фиолетового оттенка. Затем остудите зелье и приготовьте основу для теста.
Идеальным вариантом в этом случае послужит белая принтерная бумага, которая не будет вносить погрешности в цвет жидкости. Также ее преимущество заключается в том, что она хорошо впитывает отвар индикатора. Бумага должна быть нарезана полосками ориентировочно 1×5 см.
Перед тем как вы будете определять уровень pН воды, необходимо пропитать тест-полоски индикаторным раствором. Для этого процедите остывший отвар сквозь марлю и опустите в него бумагу. Следите за тем, чтобы тест-полоски пропитались равномерно. Пропитывать бумагу следует в течение 10 минут. В результате бумага должна приобрести бледно-сиреневый оттенок.
Когда бумага, пропитанная отваром, высохнет, вы можете приступать к определению уровня pН воды. Затем сложите тест-полоски в коробку или полиэтиленовый пакетик, чтобы уберечь их от влаги.
Использовать данный метод определения уровня pН очень легко. Возьмите пипетку и капните одну-две капли испытуемого раствора на тест-полоску. Подождите одну-две минуты, чтобы индикатор вступил в реакцию с бумагой. В зависимости от показателя pН воды бумага приобретет определенный оттенок, который следует сравнить с цветной шкалой, имеющей следующий вид:
 Для калибровки цветной шкалы используются вещества, которые в первоначальном виде имеют постоянный pH среды
. Ниже расположена подробная таблица этих элементов:
Для калибровки цветной шкалы используются вещества, которые в первоначальном виде имеют постоянный pH среды
. Ниже расположена подробная таблица этих элементов:
Данная таблица вам поможет в том случае, если вы захотите провести эксперимент, используя какой-либо другой индикатор (например, свекольный отвар, сок черной смородины или шелковицы).
Если полученный результат не внушает вам доверия, или вы по каким-то причинам не смогли решить проблему несбалансированного pН воды, тогда обратитесь к профессионалам.
На российском рынке присутствует немало компаний, которые занимаются разработкой систем водоочистки. Самостоятельно, без помощи профессионала, выбрать тот или иной вид фильтра для очистки воды довольно сложно. И уж тем более не стоит пытаться смонтировать систему водоочистки самостоятельно, даже если вы прочитали несколько статей в Интернете и вам кажется, что вы во всем разобрались.
Наша компания Biokit предлагает широкий выбор систем обратного осмоса, фильтры для воды и другое оборудование, способное вернуть воде из-под крана ее естественные характеристики.
Специалисты нашей компании готовы помочь вам:
подключить систему фильтрации самостоятельно;
разобраться с процессом выбора фильтров для воды;
подобрать сменные материалы;
устранить неполадки или решить проблемы с привлечением специалистов-монтажников;
найти ответы на интересующие вопросы в телефонном режиме.
Доверьте очистку воды системам от Biokit – пусть ваша семья будет здоровой!
Показатель pH и его влияние на качество питьевой воды.
Что такое pH?
pH («potentia hydrogeni» - сила водорода, или «pondus hydrogenii» - вес водорода) - это единица измерения активности ионов водорода в любом веществе, количественно выражающая его кислотность.
Данный термин появился в начале ХХ века в Дании. Показатель pH ввел датский химик Сорен Петр Лауриц Соренсен (1868-1939), хотя утверждения о некой «силе воды» встречаются и у его предшественников.
Активность водорода определяется как отрицательный десятичный логарифм концентрации водородных ионов, выраженной в молях на литр:
pH = -log
Для простоты и удобства при вычислениях был введен показатель pH. рН определяется количественным соотношением в воде ионов Н+ и ОН-, образующихся при диссоциации воды. Принято измерять уровень pH по 14-цифровой шкале.
Если в воде пониженное содержание свободных ионов водорода (рН больше 7) по сравнению с ионами гидроксида [ОН-], то вода будет иметь щелочную реакцию , а при повышенном содержании ионов Н+ (рН меньше 7) — кислую реакцию . В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга.
кислая среда: >
нейтральная среда: =
щелочная среда: >
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. В нейтральной воде показатель рН равен 7.
При растворении в воде различных химических веществ этот баланс изменяется, что приводит к изменению значения рН. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении щелочи - наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает.
рН показатель отражает степень кислотности или щелочности среды, в то время как «кислотность» и «щелочность» характеризуют количественное содержание в воде веществ, способных нейтрализовывать соответственно щелочи и кислоты. В качестве аналогии можно привести пример с температурой, которая характеризует степень нагрева вещества, но не количество тепла. Опустив руку в воду, мы можем сказать какая вода — прохладная или теплая, но при этом не сможем определить сколько в ней тепла (т.е. условно говоря, как долго эта вода будет остывать).
pH считается одним из важнейших показателей качества питьевой воды. Он показывает кислотно-щелочное равновесие и влияет на то, как будут протекать химические и биологические процессы. В зависимости от величины pH может изменяться скорость протекания химических реакций, степень коррозионной агрессивности воды, токсичность загрязняющих веществ и т.д. От кислотно-щелочного равновесия среды нашего организма напрямую зависит наше самочувствие, настроение и здоровье.
Современный человек живет в загрязненной окружающей среде. Многие приобретают и употребляют пищу, изготовленную из полуфабрикатов. Кроме этого практически каждый человек ежедневно подвергается стрессовому воздействию. Все это оказывает влияние на кислотно-щелочное равновесие среды организма, смещая его в сторону кислот. Чай, кофе, пиво, газированные напитки снижают показатель pH в организме.
Считается, что кислая среда является одной из основных причин разрушения клеток и повреждения тканей, развития заболеваний и процессов старения, росту болезнетворных организмов. В кислой среде до клеток не доходит строительный материал, разрушается мембрана.
Внешне о состоянии кислотно-щелочного равновесия крови человека можно судить по цвету его конъюнктивы в уголках глаз. При оптимальном кислотно-щелочном балансе цвет конъюнктивы ярко-розовый, если же у человека повышается щелочность крови, конъюнктива приобретает темно-розовый окрас, а при повышении кислотности окрас конъюнктивы становится бледно-розовым. При чем цвет конъюнктивы изменяется уже через 80 секунд после употребления веществ, влияющих на кислотно-щелочное равновесие.
Организм регулирует рН внутренних жидкостей, поддерживая значения на определенном уровне. Кислотно-щелочной баланс организма — это определенное соотношение кислот и щелочей, способствующее его нормальному функционированию. Кислотно-щелочной баланс зависит от сохранения относительно постоянных пропорций между межклеточными и внутриклеточными водами в тканях организма. Если кислотно-щелочное равновесие жидкостей в организме не будет поддерживаться постоянно, нормальное функционирование и сохранение жизни окажутся невозможными. Поэтому важно контролировать то, что вы потребляете.

Кислотно-щелочной баланс – это наш индикатор здоровья. Чем мы «кислее», тем скорее стареем и больше болеем. Для нормальной работы всех внутренних органов уровень рН в организме должен быть щелочным, в интервале от 7 до 9.
pH внутри нашего тела не всегда одинаков - некоторые его части более щелочные, а некоторые кислотные. Организм регулирует и поддерживает гомеостаз уровня pH лишь в отдельных случаях, например pH крови. На уровень pH почек и других органов, кислотно-щелочное равновесие которых не регулируются организмом, влияют пища и напитки, которые мы употребляем.
pH крови
Уровень pH крови поддерживается организмом в диапазоне 7.35-7.45. Нормальным показателем pH крови человека считается 7,4-7,45. Даже незначительное отклонение этого показателя влияет на способность крови переносить кислород. Если pH крови повышается до 7,5, она переносит на 75% кислорода больше. При снижении показателя pH крови до 7,3 человеку уже сложно подняться с постели. При 7,29 он может впасть в кому, если показатель pH крови снизится ниже 7,1 — человек умирает.
Уровень pH крови должен поддерживаться в здоровом диапазоне, поэтому организм использует органы и ткани для поддержания его постоянства. Вследствие этого, уровень pH крови не меняется из-за употребления щелочной или кислотной воды, но ткани и органы тела, используемые для регулировки pH крови, меняют свой pH.
pH почек
На параметр pH почек оказывает влияние вода, пища, метаболические процессы в организме. Кислотная еда (например мясные продукты, молочные продукты и др.) и напитки (сладкие газированные напитки, алкогольные напитки, кофе и пр.) приводят к низкому уровню pH в почках, потому что организм выводит излишнюю кислотность через мочу. Чем ниже уровень pH мочи, тем тяжелее приходится работать почкам. Поэтому кислотная нагрузка, приходящаяся от такой еды и напитков на почки, называется потенциальной кислотно-почечной нагрузкой.
Употребление щелочной воды приносит почкам пользу - происходит повышение уровня pH мочи, снижается кислотная нагрузка на организм. Увеличение pH мочи повышает pH организма в целом и избавляет почки от кислотных токсинов.
pH желудка
В пустом желудке содержится не больше чайной ложки желудочной кислоты, выработанной в последний прием пищи. Желудок производит кислоту по мере необходимости при употреблении пищи. Желудок не выделяет кислоту, когда человек пьет воду.
Очень полезно - пить воду на пустой желудок. Показатель pH увеличивается при этом до уровня 5-6. Увеличенный pH будет иметь мягкий антацидный эффект и приведет к увеличению количества полезных пробиотиков (благотворных бактерий). Увеличение pH желудка повышает pH организма, что ведет к здоровому пищеварению и освобождает от симптомов расстройства желудка.
pH подкожного жира
Жировые ткани организма имеют кислотный pH, поскольку в них откладываются излишние кислоты. Организму приходится хранить кислоту в жировых тканях, когда она не может быть выведена или нейтрализована иными способами. Поэтому смещение pH организма в кислую сторону - это один из факторов лишнего веса.
Позитивное влияние щелочной воды на массу тела состоит в том, что щелочная вода помогает выводить из тканей излишнюю кислоту, поскольку помогает почкам работать более рационально. Это помогает контролировать вес, поскольку многократно снижается количество кислоты, которое тело должно «хранить». Щелочная вода также улучшает результаты здоровой диеты и упражнений, помогая организму справиться с излишней кислотностью, выделяемой жировыми тканями в процессе потери веса.
Кости
У костей щелочной pH, так как они в основном состоят из кальция. Их pH постоянен, но если кровь нуждается в регулировке pH, кальций забирается из костей.
Польза, приносимая щелочной водой костям, состоит в их защите, путем снижения количества кислоты, с которым организму приходится бороться. Исследования показали, что употребление щелочной воды снижает рассасывание костей - остеопороз.
pH печени
У печени слабощелочной pH, на уровень которого влияет и пища, и напитки. Сахар и алкоголь должны быть расщеплены в печени, а это приводит к излишкам кислоты.
Польза, приносимая щелочной водой печени, состоит в наличии в такой воде антиоксидантов; установлено, что щелочная вода усиливает работу двух антиоксидантов, находящихся в печени, способствующих более эффективному очищению крови.
pH организма и щелочная вода
Щелочная вода позволяет частям тела, сохраняющим pH крови, работать с большей производительностью. Повышение уровня pH в частях тела, отвечающих за поддержание pH крови, поможет этим органам оставаться здоровыми и работать оперативно.
Между приемами пищи Вы можете помочь Вашему организму нормализовать показатель pH, употребляя щелочную воду. Даже небольшое увеличение pH может оказать огромное влияние на состояние здоровья.
По данным исследований японских ученых, показатель pH питьевой воды, находящийся в диапазоне 7-8, повышает продолжительность жизни населения на 20-30%.
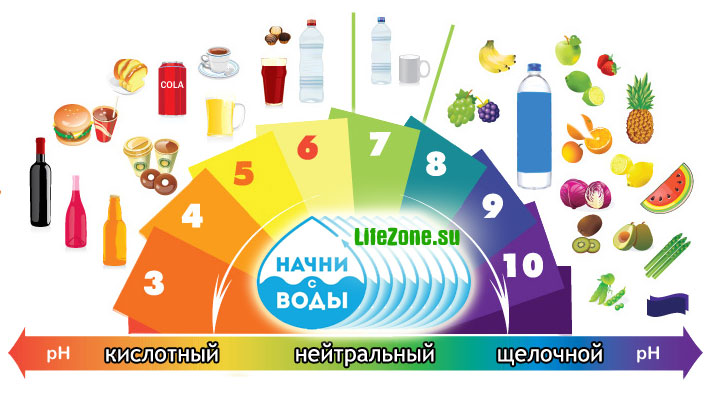
В зависимости от уровня рН воды можно условно разделить на несколько групп:
Сильнокислые воды < 3
кислые воды 3 — 5
слабокислые воды 5 — 6.5
нейтральные воды 6.5 — 7.5
слабощелочные воды 7.5 — 8.5
щелочные воды 8.5 — 9.5
сильнощелочные воды > 9.5
Обычно уровень рН питьевой водопроводной воды находится в пределах, при которых он непосредственно не влияет на потребительские качества воды. В речных водах pH обычно находится в пределах 6.5-8.5, в атмосферных осадках 4.6-6.1, в болотах 5.5-6.0, в морских водах 7.9-8.3.
ВОЗ не предлагает какой-либо рекомендуемой по медицинским показателям величины для рН. Известно, что при низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях (рН>11) вода приобретает характерную мылкость, неприятный запах, способна вызывать раздражение глаз и кожи. Именно поэтому для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9.
|
|||||||||||||||||||||||||||||||||||||||||||||||



Интересно знать: Немецкий биохимик ОТТО ВАРБУРГ, удостоенный в 1931 Нобелевской премии по физиологии и медицине доказал, что недостаток кислорода (кислая среда pH<7.0) в тканях приводит к изменению нормальных клеток в злокачественные.
Ученый обнаружил, что раковые клетки теряют способность к развитию в среде, насыщенной свободным кислородом с показателем pH=7,5 и выше! Это означает, что когда жидкости в организме становятся кислыми, стимулируется развитие рака.
Его последователи в 60-х годах прошлого столетия доказали, что любая патогенная флора теряет способность размножаться при pH=7,5 и выше, и наша иммунная система легко справляется с любыми агрессорами!
Для сохранения и поддержания здоровья нам необходима правильная щелочная вода (рН=7.5 и выше). Это позволит лучше сохранять кислотно-щелочное равновесие жидкостей организма, так как основные жизненные среды имеют слабощелочную реакцию.
Уже при нейтральной биологической среде организм может обладать удивительной способностью к самоисцелению.

Не знаете где можно взять правильную воду ? Я подскажу!

Обратите внимание:
Нажатие на кнопку «Узнать » не ведет к каким-либо финансовым тратам и обязательствам.
Вы лишь получите информацию о доступности правильной воды в Вашем регионе ,
а так же получите уникальную возможность бесплатно стать членом клуба здоровых людей
и получить скидку 20% на все предложения + накопительный бонус.

Вступи в международный клуб здоровья Coral Club , получи БЕСПЛАТНО дисконтную карту, возможность участия в акциях, накопительный бонус и другие привилегии!

Кислотность (лат. aciditas ) - характеристика активности ионов водорода в растворах и жидкостях.
В медицине кислотность биологических жидкостей (крови, мочи, желудочного сока и других) является диагностически важным параметром состояния здоровья пациента. В гастроэнтерологии, для правильного диагностирования целого ряда заболеваний, например, пищевода и желудка, одномоментная или даже средняя величина кислотности не является значимой. Чаще всего важно понимание динамики изменения кислотности в течение суток (ночная кислотность нередко отличается от дневной) в нескольких зонах органа. Иногда важно знать изменение кислотности, как реакцию на определенные раздражители и стимуляторы.
Водородный показатель pH
В растворах неорганические вещества: соли, кислоты и щелочи разделяются на составляющие их ионы. При этом ионы водорода H + являются носителями кислотных свойств, а ионы OH − – носителями щелочных свойств. В сильно разбавленных растворах кислотные и щелочные свойства зависят от концентраций ионов H + и OH − . В обычных растворах кислотные и щелочные свойства зависят от активностей ионов а Н и а OН, то есть от тех же концентраций, но с поправкой на коэффициент активности γ, который определяется экспериментально. Для водных растворов действует уравнение равновесия: а Н × а OН = К w , где К w – константа, ионное произведение воды (К w = 10 − 14 при температуре воды 22 °C). Из этого уравнения следует, что активность ионов водорода H + и активность ионов OH − связаны между собой. Датским биохимиком С.П.Л. Серенсеном в 1909 году был предложен водородный показать рН , равный по определению десятичному логарифму активности водородных ионов, взятому с минусом (Рапопорт С.И. и др.):
рН = - lg (а Н)
.
Исходя из того, что в нейтральной среде а Н = а OН и из выполнения равенства для чистой воды при 22 °С: а Н × а OН = К w = 10 − 14 , получаем, что кислотность чистой воды при 22 °С (то есть нейтральная кислотность) = 7 ед. pH.
Растворы и жидкости в отношении их кислотности считаются:
- нейтральными при рН = 7
- кислыми при pH < 7
- щелочными при рН > 7
Некоторые заблуждения
Если кто-то из пациентов говорит, что у него «нулевая кислотность», то это не более, чем оборот речи, означающий, скорее всего, что у него нейтральное значение кислотности (рН=7). В организме человека величина показателя кислотности не может быть меньше 0,86 рН. Также распространено заблуждение, что величины кислотности могут быть только в диапазоне от 0 до 14 pH. В технике возможен показатель кислотность и отрицательный, и больше 20.Когда говорят о кислотности кого-либо органа, важно при этом понимать, что часто в различных частях органа кислотность может значительно отличаться. Кислотность содержимого в просвете органа и кислотность на поверхности слизистой оболочки органа также часто бывает не одинаковой. Для слизистой оболочки тела желудка характерно, что кислотность на поверхности слизи, обращенной в просвет желудка кислотность 1,2–1,5 рН, а на стороне слизи, обращённой к эпителию - нейтральная (7,0 рН).
Величина рН для некоторых продуктов и воды
В таблице ниже указаны величины кислотности некоторых распространенных продуктов и чистой воды при разной температуре:| Продукт | Кислотность, ед. рН |
| Лимонный сок | 2,1 |
| Вино | 3,5 |
| Томатный сок | 4,1 |
| Апельсиновый сок | 4,2 |
| Черный кофе | 5,0 |
| Чистая вода при 100 °С |
6,13 |
|
Чистая вода при 50 °С |
6,63 |
| Свежее молоко | 6,68 |
| Чистая вода при 22 °С |
7,0 |
| Чистая вода при 0° С | 7,48 |
Кислотность и пищеварительные ферменты
Очень многие процессы в организме невозможны без участия специальных белков – ферментов, которые катализируют химические реакции в организме, не подвергаясь при этом химическим превращениям. Пищеварительный процесс не возможен без участия разнообразных пищеварительных ферментов, расщепляющих разные органические молекулы пищи и действующих только в узком диапазоне кислотности (своем для каждого фермента). Важнейшие протеолитические ферменты (расщепляющие белки пищи) желудочного сока: пепсин , гастриксин и химозин (реннин) продуцируются в неактивной форме – в виде проферментов и позже активируется соляной кислотой желудочного сока. Пепсин наиболее активен в сильнокислой среде, с pH от 1 до 2, гастриксин имеет максимум активности при рН 3,0–3,5, химозин, расщепляющий белки молока до нерастворимого белка казеина, имеет максимум активности при рН 3,0–3,5.Протеолитический ферменты, выделяемые поджелудочной железой и "действующие" в двенадцатиперстной кишке: трипсин имеющий оптимум действия в слабощелочной среде, при pH 7,8–8,0, близкий к нему по функциональности химотрипсин наиболее активен в среде с кислотностью до 8,2. Максимум активности карбоксипептидаз А и В 7,5 рН. Близкие значения максимальной и у других ферментов, выполняющих пищеварительные функции в слабощелочной среде кишечника.
Пониженная или повышенная кислотность по отношению к норме в желудке или двенадцатиперстной кишке, таким образом, приводит к существенному снижению активности тех или ферментов или даже их исключению из пищеварительного процесса, и, как следствие к проблемам с пищеварением.
Кислотность слюны и полости рта
Кислотность слюны зависит от скорости слюноотделения. Обычно кислотность смешанной слюны человека равна 6,8–7,4 pH, но при большой скорости слюноотделения достигает 7,8 pH. Кислотность слюны околоушных желёз равна 5,81 pH, подчелюстных - 6,39 pH.У детей в среднем кислотность смешанной слюны равна 7,32 pH, у взрослых - 6,40 pH (Римарчук Г.В. и др.).
Кислотность зубного налета зависит от состояния твердых тканей зубов. Будучи нейтральной у здоровых зубов, она смещается в кислую сторону, в зависимости от степени развития кариеса и возраста подростков. У 12-летних подростков с начальной стадией кариеса (предкариесом) кислотность зубного налета равна 6,96 ± 0,1 pH, у 12–13-летних подростков со среднем кариесом кислотность зубного налета от 6,63 до 6,74 pH, у 16-летних подростков при поверхностном и среднем кариесе кислотность зубного налета равна, соответственно, 6,43 ± 0,1 pH и 6,32 ± 0,1 pH (Кривоногова Л.Б.).
Кислотность секрета глотки и гортани
Кислотность секрета глотки и гортани у здоровых и больных хроническим ларингитом и фаринголарингеальным рефлюксом различна (А.В. Лунев):|
Группы обследованных |
Место измерения рН |
|||||||||||||||||||||||||
|
Глотка
, |
Гортань
, |
|||||||||||||||||||||||||
|
Здоровые лица |
||||||||||||||||||||||||||
| Больные хроническим ларингитом без ГЭРБ |
На рисунке выше дан график кислотности в пищеводе здорового человека, полученный с помощью внутрижелудочной рН-метрии (Рапопорт С.И.). На графике хорошо наблюдаемы гастроэзофагеальные рефлюксы – резкие уменьшения кислотности до 2–3 рН, в данном случае являющиеся физиологичными. Кислотность в желудке. Повышенная и пониженная кислотность Максимальная наблюдаемая кислотность в желудке 0,86 рН, что соответствует кислотопродукции 160 ммоль/л. Минимальная кислотность в желудке 8,3 рН, что соответствует кислотности насыщенного раствора ионов HCO 3 - . Нормальная кислотность в просвете тела желудка натощак 1,5–2,0 рН. Кислотность на поверхности эпителиального слоя, обращённого в просвет желудка 1,5–2,0 рН. Кислотность в глубине эпителиального слоя желудка около 7,0 рН. Нормальная кислотность в антруме желудка 1,3–7,4 рН. Максимальная наблюдаемая кислотность в желудке 0,86 рН, что соответствует кислотопродукции 160 ммоль/л. Минимальная кислотность в желудке 8,3 рН, что соответствует кислотности насыщенного раствора ионов HCO 3 - . Нормальная кислотность в просвете тела желудка натощак 1,5–2,0 рН. Кислотность на поверхности эпителиального слоя, обращённого в просвет желудка 1,5–2,0 рН. Кислотность в глубине эпителиального слоя желудка около 7,0 рН. Нормальная кислотность в антруме желудка 1,3–7,4 рН. Причиной многих болезней органов пищеварительного тракта является дисбаланс процессов кислотопродукции и кислотонейтрализации. Длительная гиперсекреции соляной кислоты или недостаточность кислотонейтрализации, и, как следствие, повышенная кислотность в желудке и/или двенадцатиперстной кишке, вызывает так называемые кислотозависимые заболевания. В настоящее время к ним относят: пептическую язву желудка и двенадцатиперстной кишки , гастроэзофагеальную рефлюксную болезнь (ГЭРБ) , эрозивно-язвенные поражения желудка и двенадцатиперстной кишки на фоне приема аспирина или нестероидных противовоспалительных препаратов (НПВП), синдром Золлингера-Эллисона, гастриты и гастродуодениты с повышенной кислотностью и другие. Пониженная кислотность наблюдается при анацидных или гипоацидных гастрите или гастродуодените, а также при раке желудка. Гастрит (гастродуоденит) называется анацидным или гастритом (гастродуоденитом) с пониженной кислотностью, если кислотность в теле желудка составляет примерно 5 или больше ед. pH. Причиной пониженной кислотности часто бывает атрофия париетальных клеток в слизистой оболочке или нарушения в их функциях. Выше дан график кислотности (суточная рН-грамма) тела желудка здорового человека (пунктирная линия) и больного язвой двенадцатиперстной кишки (сплошная линия). Моменты приема пищи отмечены стрелками с надписью "Еда". На графике видно кислотонейтрализующее действие пищи, а также повышенная кислотность желудка при язве двенадцатиперстной кишки (Яковенко А.В.). Кислотность в кишечникеНормальная кислотность в луковице двенадцатиперстной кишки 5,6–7,9 рН. Кислотность в тощей и подвздошной кишках нейтральная или слабощелочная и находится в пределах от 7 до 8 рН. Кислотность сока тонкой кишки 7,2–7,5 рН. При усилении секреции достигает 8,6 рН. Кислотность секрета дуоденальных желез - от рН от 7 до 8 рН.
Кислотность калаКислотность кала здорового человека, питающегося смешанной пищей обусловлена жизнедеятельность микрофлоры толстой кишки и равна 6,8–7,6 рН. Нормальной считается кислотность кала в диапазоне от 6,0 до 8,0 рН. Кислотность мекония (первородного кала новорожденных) - около 6 рН. Отклонения от нормы при кислотности кала:
Кислотность кровиКислотность плазмы артериальной крови человека колеблется в пределах от 7,37 до 7,43 рН, составляя в среднем 7,4 рН. Кислотно-щелочное равновесие в крови человека является одним из самых стабильных параметров, поддерживающее кислые и щелочные компоненты в определенном равновесии в очень узких границах. Даже небольшой сдвиг от указанных пределов может привести к тяжелой патологии. При сдвиге в кислотную сторону возникает состояние, называемое ацидозом, в щелочную - алколозом. Изменение кислотности крови выше 7,8 рН или ниже 6,8 рН несовместимо с жизнью.Кислотность венозной крови - 7,32–7,42 рН. Кислотность эритроцитов составляет 7,28–7,29 рН. Кислотность мочиУ здорового человека при нормальном питьевом режиме и сбалансированном питании кислотность мочи находится в пределах от 5,0 до 6,0 рН, но может колебаться от 4,5 до 8,0 рН. Кислотность мочи новорожденного в возрасте до месяца в норме - от 5,0 до 7,0 рН.Кислотность мочи повышается, если в рационе человека преобладает мясная пища, богатая белками. Увеличивает кислотность мочи тяжелая физическая работа. Молочно-растительная диета приводит к тому, что моча становится слабощелочной. Повышение кислотности мочи отмечается при повышенной кислотности желудка . Пониженная кислотность желудочного сока не влияет на кислотность мочи. Изменение кислотности мочи чаще всего соответствует изменению . Кислотность мочи изменяется при многие заболевания или состояниях организма, поэтому определение кислотности мочи является важным диагностическим фактором. Кислотность влагалищаНормальная кислотность влагалища женщины колеблется от 3,8 до 4,4 pH и в среднем составляет 4,0–4,2 pH. Кислотность влагалища при различных заболеваниях:
Публикации для профессионалов здравоохранения, затрагивающие проблематику кислотности в женских половых органах
Кислотность спермыНормальный уровень кислотности спермы находится в пределах от 7,2 до 8,0 рН. Отклонения от этих значений само по себе не рассматривается как патология. В то же время в совокупности с другими отклонениями может свидетельствовать о наличии заболевания. Увеличение уровня рН спермы происходит при инфекционном процессе. Резко щелочная реакция спермы (кислотность примерно 9,0–10,0 рН) свидетельствует о патологии предстательной железы. При закупорке выводных протоков обоих семенных пузырьков отмечается кислая реакция спермы (кислотность 6,0–6,8 рН). Оплодотворяющая способность такой спермы снижена. В кислой среде сперматозоиды теряют подвижность и погибают. Если кислотность семенной жидкости становится меньше 6,0 рН, сперматозоиды полностью теряют подвижность и погибают.Кислотность кожиПоверхность кожи покрыта воднолипидной кислотной мантией или мантией Маркионини , состоящей из смеси кожного сала и пота, в которую добавлены органические кислоты - молочная, лимонная и другие, образованные в результате биохимических процессов, протекающих в эпидермисе. Кислотная воднолипидная мантия кожи является первым барьером защиты от микроорганизмов. У большинства людей в норме кислотность мантии равна 3,5–6,7 рН. Бактерицидное свойство кожи, придающее ей способность противостоять микробной инвазии, обусловлено кислой реакцией кератина, своеобразным химическим составом кожного сала и пота, наличием на ее поверхности защитной воднолипидной мантии с высокой концентрацией водородных ионов. Входящие в ее состав низкомолекулярные жирные кислоты, в первую очередь гликофосфолипиды и свободные жирные кислоты, обладают бактериостатическим эффектом, селективным для патогенных микроорганизмов. Поверхность кожи заселена нормальной симбиотической микрофлорой, способной к существованию в кислой среде: Staphylococcus epidermidis , Staphylococcus aureus , Propionibacterium acnes и другие. Некоторые из этих бактерий сами вырабатывают молочную и другие кислоты, внося свой вклад в формирование кислотной мантии кожи.Верхний слой эпидермиса (кератиновые чешуйки) имеет кислотность с величиной рН от 5,0 до 6,0. При некоторых кожных заболеваниях величина кислотности изменяется. Например, при грибковых заболеваниях рН возрастает до 6, при экземе до 6,5, при угревой сыпи до 7. Кислотность других биологических жидкостей человекаКислотность жидкостей внутри человеческого организма в норме совпадает с кислотностью крови и находится в пределах от 7,35 до 7,45 pH. Кислотность некоторых других биологических жидкостей человека в норме приведена в таблице:На фотографии справа: буферные растворы с рН=1,2 и рН=9,18 для калибровки | |||||||||||||||||||||||||
pH фактор – это измерение относительной кислотности или щелочности раствора. Значение рН 7 считается нейтральным раствором, кислые растворы имеют значения ниже 7, а щелочные - выше 7. Значение рН может быть измерено pH-метром, переносным pH-метром или с помощью лакмусовой бумажки. Измерение pH фактора обеспечивает числовое обозначение относительной кислотности или щелочности, что является важным параметром в контроле раствора.
Для того, чтобы раствор выполнял свои функции как необходимо, должен быть известен желаемый pH фактор, и раствором тогда можно управлять. Для иллюстрации рассмотрим производство желе. Для превращения фруктов в желе смесь должна быть немного кислой. При pH ниже 2,6 смесь не будет превращаться в желе; при значении 2:6 образуется белый осадок, и желе не имеет рыночного вида; при значении 2,8 происходит отделение капелек воды от смеси; при значении 3,1 смесь образует желе максимальной консистенции; при значении 3,2 образуется желе средней консистенции, а при 3,3 желе будет жидким. При значении рН выше 3,5 желе из смеси вообще не получиться.
Так в пределах нескольких десятых частей pH фактора желе из смеси не образуется, затем получается максимальная консистенция, потом желе опять не получается. Данный пример иллюстрирует важность жесткого контроля pH фактора раствора.
Есть широкий диапазон кислот, от серной кислоты, которая может растворять металл до борной кислоты, которая годится для промывки глаз. Все кислоты образуют в растворе ионы водорода (H+). Степень кислотности – это числовое обозначение концентрации ионов водорода. Выражаясь языком химии, числовые обозначения концентраций ионов водорода представляют собой обычно чрезвычайно малые фракции, например, 1/10 000 000. Масштаб pH фактора был разработан, чтобы избежать использования таких неудобных чисел. Масштаб pH фактора определен математически как отрицательный логарифм концентрации ионов водорода или степени, в которую должна быть возведена 10, чтобы равняться концентрации ионов водорода. Название рН происходит от термина «степень водорода». Математическое выражение предоставляет нам удобный масштаб от 0 для кислого раствора удельной прочности до 7 для нейтрального раствора чистой воды.
Щелочи обязаны своей щелочностью гидроксильным ионам (ОН-), которые они образуют в растворе. Щелочность может быть измерена в том же самом масштабе, как и кислотность, от 7 до 14.
Проще говоря, любое число ниже 7,0 – это кислота и при каждой единице уменьшения этого значения увеличивается интенсивность (ионная концентрация H+) кислоты на фактор 10Х. Любое число выше 7,0 считается щелочью, и на каждую единицу увеличения этого значения увеличивается интенсивность (ионная концентрация ОН-) щелочи на фактор 10Х. В растворе, где присутствует одинаковое количество ионов Н+ и ионов ОН-, pH фактор равняется 7,0.
Водопроводная вода может быть немного щелочной вследствие добавок каустической соды, чтобы сделать воду более приятной для питья. Надлежащее измерение и регулирование воды имеют существенное значение в процессе предварительной обработки. Для обеспечения точности измерений рН-метр должен быть должным образом откалиброван.
Калибровка одноточечным методом описана ниже.
1) Подключите электрод pH к прибору и снимите защитный колпачок с электрода.
2) Промойте электрод pH дистиллированной водой и погрузите его в буферный раствор 7,00.*
3) Включите прибор, установив трехпозиционный переключатель в положение ON (включено).
4) Установите температурный контроль прибора на температуру буферного раствора (используйте термометр Tru GT 100R или другой подходящий термометр, чтобы измерить температуру буферного раствора).
5) Отрегулируйте контроль стандартизации для считывания значения, соответствующего температуре буферного раствора. Буферные значения приводятся в Таблице 1.
6) Достаньте электрод из буферного раствора и промойте дистиллированной водой.
Прибор измерения pH теперь откалиброван и готов к применению.
Кнопка регулирования температуры на приборе должна устанавливаться на температуру раствора, значение рН которого измеряется.
Нельзя допустить высыхание электрода. Если он не используется, электрод должен быть погружен в буферный раствор. Электрод не должен использоваться в растворах с температурой выше 140°Ф (60°C) и должен быть защищен от замораживания. Электрод должен промываться дистиллированной водой до перенесения в буферный раствор из измеряемого раствора. Влагу с электрода необходимо стряхивать, чтобы уменьшить загрязнение раствора при перенесении электрода из одного раствора в другой.
Если на наконечнике электрода образовалась пленочное покрытие, пробуйте удалить его, активно мешая в моющем растворе или опыляя его из баллончика. Если это не сработает, и прибор медленно или неправильно реагирует, можно аккуратно очистить стеклянный сосуд мягкой щеткой. Если и это не даст результата, замените сосуд или прибор.
Значения рН буферных растворов следует периодически проверять, сравнивая их со значениями в свежих буферных растворах. Замените раствор, когда разница значений рН будет достигать 0,1 или больше.
Одно из важнейших свойств водных растворов их кислотность (или щелочность), которая определяется концентрацией ионов Н + и ОН (см . ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ЭЛЕКТРОЛИТЫ ). Концентрации этих ионов в водных растворах связаны простой зависимостью = К w ; (квадратными скобками принято обозначать концентрацию в единицах моль/л). Величина Kw называется ионным произведением воды и при данной температуре постоянна. Так, при 0 о С она равна 0,11 Ч 10 14 , при 20 о С 0,69 Ч 10 14 , а при 100 о С 55,0 Ч 10 14 . Чаще всего пользуются значением K w при 25 о С, которое равно 1,00 Ч 10 14 . В абсолютно чистой воде, не содержащей даже растворенных газов, концентрации ионов Н + и ОН равны (раствор нейтрален). В других случаях эти концентрации не совпадают: в кислых растворах преобладают ионы Н + , в щелочных ионы ОН . Но их произведение в любых водных растворах постоянно. Поэтому если увеличить концентрацию одного из этих ионов, то концентрация другого иона уменьшится во столько же раз. Так, в слабом растворе кислоты, в котором = 10 5 моль/л, = 10 9 моль/л, а их произведение по-прежнему равно 10 14 . Аналогично в щелочном растворе при = 3,7 Ч 10 3 моль/л = 10 14 /3,7 Ч 10 3 = 2,7 Ч 10 11 моль/л.Из сказанного следует, что можно однозначно выразить кислотность раствора, указав концентрацию в нем только ионов водорода. Например, в чистой воде = 10
7
моль/л. На практике оперировать такими числами неудобно. Кроме того, концентрации ионов Н
+
в растворах могут отличаться в сотни триллионов раз примерно от 10
15
моль/л (крепкие растворы щелочей) до 10 моль/л (концентрированная соляная кислота), что невозможно изобразить ни на каком графике. Поэтому давно договорились для концентрации ионов водорода в растворе указывать только показатель степени 10, взятый с обратным знаком; для этого концентрацию следует выразить в виде степени 10х, без множителя, например, 3,7
Ч
10
3
= 10
2,43
. (При более точных расчетах, особенно в концентрированных растворах, вместо концентрации ионов используют их активности.) Этот показатель степени получил название водородного показателя, а сокращенно рН от обозначения водорода и немецкого слова Potenz математическая степень. Таким образом, по определению, рН = lg[Н
+
]; эта величина может изменяться в небольших пределах всего от 1 до 15 (а чаще от 0 до 14). При этом изменению концентрации ионов Н
+
в 10 раз соответствует изменение рН на одну единицу. Обозначение рН ввел в научный обиход в 1909 датский физикохимик и биохимик С.П.Л.Сёренсен, который занимался в то время изучением процессов, происходящих при сбраживании пивного солода, и их зависимостью от кислотности среды.
При комнатной температуре в нейтральных растворах рН = 7, в кислых растворах рН 7. Приблизительно значение рН водного раствора можно определить с помощью индикаторов. Например, метиловый оранжевый при рН 4,4 желтый; лакмус при рН 8 синий и т.д. Более точно (до сотых долей) значение рН можно определить с помощью специальных приборов рН-метров. Такие приборы измеряют электрический потенциал специального электрода, погруженного в раствор; этот потенциал зависит от концентрации ионов водорода в растворе, и его можно измерить с высокой точностью. Интересно сравнить значения рН растворов различных кислот, оснований, солей (при концентрации 0,1 моль/л), а также некоторых смесей и природных объектов. Для малорастворимых соединений, отмеченных звездочкой, приведены рН насыщенных растворов. Таблица 1. Водородные показатели для растворов Природная вода всегда имеет кислую реакцию (рН 2
+ Н
2
О
«
Н
+
+ НСО
3
2
. Если насытить воду углекислым газом при атмосферном давлении, рН полученной «газировки» будет равен 3,7; такую кислотность имеет примерно 0,0007%-ный раствор соляной кислоты желудочный сок намного кислее! Но даже если повысить давление CO
2
над раствором до 20 атм, значение pH не опускается ниже 3,3. Это значит, что газированную воду (в умеренных количествах, конечно) можно пить без вреда для здоровья, даже если она насыщена углекислым газом.
Определенные значения рН имеют исключительно большое значение для жизнедеятельности живых организмов. Биохимические процессы в них должны протекать при строго заданной кислотности. Биологические катализаторы ферменты способны работать только в определенных пределах рН, а при выходе за эти пределы их активность может резко снижаться. Например, активность фермента пепсина, который катализирует гидролиз белков и способствует таким образом перевариванию белковой пищи в желудке, максимальна при значениях рН около 2. Поэтому для нормального пищеварения необходимо, чтобы желудочный сок имел довольно низкие значения рН: в норме 1,531,67. При язвенной болезни желудка рН понижается в среднем до 1,48, а при язве двенадцатиперстной кишки может доходить даже до 105. Точное значение рН желудочного сока определяют путем внутрижелудочного исследования (рН-зонд). Если у человека понижена кислотность, В клетках организма рН имеет значение около 7, во внеклеточной жидкости 7,4. Нервные окончания, которые находятся вне клеток, очень чувствительны к изменению рН. При механических или термических повреждениях тканей стенки клеток разрушаются и их содержимое попадает на нервные окончания. В результате человек чувствует боль. Скандинавский исследователь Олаф Линдал проделал такой эксперимент: с помощью специального безыгольного инъектора человеку впрыскивали сквозь кожу очень тонкую струйку раствора, которая не повреждала клетки, но действовала на нервные окончания. Было показано, что боль вызывают именно катионы водорода, причем с уменьшением рН раствора боль усиливается. Аналогично непосредственно «действует на нервы» и раствор муравьиной кислоты, который жалящие насекомые или крапива впрыскивают под кожу. Разным значением рН тканей объясняется также, почему при некоторых воспалениях человек чувствует боль, а при некоторых нет. Интересно, что впрыскивание под кожу чистой воды дало особенно сильную боль. Объясняется это странное на первый взгляд явление так: клетки при контакте с чистой водой в результате осмотического давления разрываются и их содержимое воздействует на нервные окончания. В очень узких пределах должно оставаться значение рН крови; даже небольшое ее подкисление (ацидоз) или защелачивание (алкалоз) может привести к гибели организма. Ацидоз наблюдается при таких заболеваниях как бронхит, недостаточность кровообращения, опухоли легких, пневмония, диабет, лихорадка, поражения почек и кишечника. Алколоз же наблюдается при гипервентиляции легких (или при вдыхании чистого кислорода), при анемии, отравлении СО, истерии, опухоли мозга, избыточном потреблении питьевой соды или щелочных минеральных вод, приеме диуретических лекарств. Интересно, что рН артериальной крови в норме должно быть в пределах 7,377,45, а венозной 7,347,43. Различные микроорганизмы также весьма чувствительны к кислотности среды. Так, патогенные микробы быстро развиваются в слабощелочной среде, тогда как кислую среду они не выдерживают. Поэтому для консервирования (маринование, соление) продуктов используют, как правило, кислые растворы, добавляя в них уксус или пищевые кислоты. Большое значение имеет правильный подбор рН и для химико-технологических процессов. Поддержать нужное значение рН, не дать ему заметно отклониться в ту или другую сторону при изменении условий возможно при использовании так называемых буферных (от англ. buff смягчать толчки) растворов. Такие растворы часто представляют собой смесь слабой кислоты и ее соли или слабого основания и его соли. Подобные растворы «сопротивляются» в определенных пределах (которые называются емкостью буфера) Многие природные жидкости обладают буферными свойствами. Примером может служить вода в океане, буферные свойства которой во многом обусловлены растворенным углекислым газом и гидрокарбонат-ионами НСО Клеточная жидкость, кровь также являются примерами природных буферных растворов. Так, кровь содержит около 0,025 моль/л углекислого газа, причем его содержание у мужчин примерно на 5% выше, чем у женщин. Примерно такая же в крови концентрация гидрокарбонат-ионов (их тоже больше у мужчин). При исследовании почвы рН является одной из наиболее важных характеристик. Разные почвы могут иметь рН от 4,5 до 10. По значению рН, в частности, можно судить о содержании в почве питательных веществ, а также о том, какие растения могут успешно расти на данной почве. Например, рост фасоли, салата, черной смородины затрудняется при рН почвы ниже 6,0; капусты ниже 5,4; яблони ниже 5,0; картофеля ниже 4,9. Кислые почвы обычно менее богаты питательными веществами, поскольку хуже удерживают в себе катионы металлов, необходимые растениям. Например, попавшие в почву ионы водорода вытесняют из нее связанные ионы Са Для раскисления кислых почв используют их известкование внесение веществ, постепенно связывающих избыток кислоты. Таким веществом могут служить природные минералы мел, известняк, доломит, а также известь, шлак с металлургических заводов. Количество внесенного раскислителя зависит от буферной емкости почвы. Например, для известкования глинистой почвы требуется больше раскисляющих веществ, чем для песчаной. Большое значение имеют измерения рН дождевой воды, которая может оказаться довольно кислой из-за присутствия в ней серной и азотной кислот. Эти кислоты образуются в атмосфере из оксидов азота и серы (IV), которые выбрасываются с отходами многочисленных производств, транспорта, котельных и ТЭЦ. Известно, что кислотные дожди с низким значением рН (менее 5,6) губят растительность, живой мир водоемов. Поэтому постоянно ведется контроль рН дождевой воды.
Таблица позволяет сделать ряд интересных наблюдений. Значения рН, например, сразу показывают сравнительную силу кислот и оснований. Хорошо видно также сильное изменение нейтральной среды в результате гидролиза солей, образованных слабыми кислотами и основаниями, а также при диссоциации кислых солей.
Раствор
РН
HCl
1,0
H 2 SO 4
1,2
H 2 C 2 O 4
1,3
NaHSO 4
1,4
Н 3 РО 4
1,5
Желудочный сок
1,6
Винная кислота
2,0
Лимонная кислота
2,1
HNO 2
2,2
Лимонный сок
2,3
Молочная кислота
2,4
Салициловая кислота
2,4
Столовый уксус
3,0
Сок грейпфрута
3,2
СО 2
3,7
Яблочный сок
3,8
H 2 S
4,1
Моча
4,8–7,5
Черный кофе
5,0
Слюна
7,4–8
Молоко
6,7
Кровь
7,35–7,45
Желчь
7,8–8,6
Вода океанов
7,9–8,4
Fe(OH) 2
9,5
MgO
10,0
Mg(OH) 2
10,5
Na 2 CO 3
11
Ca(OH) 2
11,5
NaOH
13,0
Добиш.
Электрохимические константы
. М., 1980
Чиркин А. и др.
Диагностический справочник терапевта
. Минск. 1993